美国USP纯化水的水纯化、贮存和分配系统的验证与确认要求
【苏州水处理设备http://www.tjxqcs.com】建立制药用水净化、贮存和分配系统的可靠性,要求一个适当的监测与观察时期。一般地,在保持纯化水与注射用水的化学纯度方面几乎没有问题。然而用电导率与TOC来定义化学纯度的出现使得使用者可以更加量化的评估水的化学纯度,以及作为日常的预处理系统维护保养与再生的功能的变异性。但这些单元操作(例如热交换器和使用点软管)可能会损害水(在系统中的以及从控制良好的水系统中流出的水)的化学纯度。因此,一段时间的水的化学纯度的连续性的评估必须是验证程序的一部分。然而,虽然化学纯度控制的很好,但由于在化学纯化期间和纯化之后出现的现象使得始终符合已制定的微生物质量标准,常常是更加困难。在一个有代表性的方案中,(在建立每一个单元操作、使用点和取样点建立操作标准后)应包含至少在一个月当中对于主要工艺使用点每天进行集中地取样并检测。
水系统验证的一个检查方面是水向其使用位置的输送。如果从分配系统的出口到水使用点(通常是软管)的输送过程被定义为外部水系统,那么此输送过程仍需要被验证,验证对水质量不得影响的不适于使用的程度。因为日常的微生物监测是针对相同的输送过程和作为日常水使用(见取样考虑的事情)的部件(例如软管和热交换器)来进行的,在分配系统验证范围内包括这个水输送过程是有一些道理的。
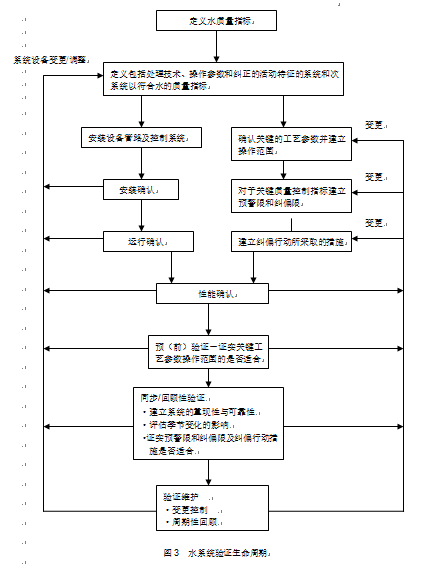
验证是一个程序,通过此程序获得和记录一个高度保证的证明,证明一个特定的工艺将连续生产出符合已建立的一系列质量指标的产品。在验证非常早的阶段之前和验证期间,制定关键的工艺参数和它们的操作范围。验证程序确认和证明设备的设计、安装、运行以及性能。在系统被定义时开始,并且通过几个阶段来进行:安装确认、运行确认以及性能确认。一个典型水系统验证生产周期的图示描述如图3所示。
一个验证计划通常包括以下几下步骤:
(1) 制定成品水与源水的质量标准;
(2) 定义适当的单元操作以及它们的操作参数,以达到预期的来自源水的成品水的质量属性;
(3) 选择管路、设备、控制与监测技术;
(4) 建立安装确认(IQ),包括:仪器校验,检查以确认图纸是否准确描述水系统的构造结构,(如必要)进行专门的试验以确认安装是否符合设计要求;
(5) 建立运行确认(OQ),包括:检测和检查以确认设备,系统报警和控制是否正常运转,建立适当的预警限和纠偏限。(这个确认阶段可能与下一步的某些方面相重叠);
(6) 建立预性能确认(PQ):确认关键工艺参数操作范围是否适合(在此验证阶段,证实关键质量属性与操作参数的预警限和纠偏限);
工业纯水设备, 苏州水处理设备,苏州医用纯水设备 ,医用水处理设备。
- 上一篇:美国USP纯化水与注射用水系统要求 2020/3/16
- 下一篇:美国药典USP对纯化水的类型定义 2020/3/16
